從原理到實(shí)操|深度全解抗體純化蛋白A親和層析工藝,收率再上新高度

Ⅰ
抗體下游工藝流程的概況
近些年單抗市場(chǎng)發(fā)展迅速,從2008至2022年,全球生物制品市場(chǎng)份額從17%增長(zhǎng)至30%,大約50%生物制品銷售額來自于抗體及其Fc融合蛋白。近些年,中國(guó)單抗藥物市場(chǎng)呈爆發(fā)性增長(zhǎng)趨勢(shì),2022年銷售額已達(dá)1100億,預(yù)計(jì)2023年將突破1500億,而國(guó)產(chǎn)單抗藥物也陸續(xù)實(shí)現(xiàn)突破,近些年不斷有新的單抗藥物上市。
但在單抗快速發(fā)展的同時(shí),制藥企業(yè)也面臨著新的挑戰(zhàn)。首先是降低生產(chǎn)成本,由于熱門靶點(diǎn)有限,可能同一款單抗藥物有多個(gè)公司在同時(shí)研發(fā)藥物,制藥公司面臨著激烈的市場(chǎng)競(jìng)爭(zhēng),同時(shí)由于國(guó)家4+7帶量采購(gòu)的政策的發(fā)布,迫使藥企迫切追求降低生產(chǎn)成本。其次是提高生產(chǎn)效率,除部分熱門靶點(diǎn)藥物外,大部分靶點(diǎn)藥物市場(chǎng)需求量小。最后是產(chǎn)品質(zhì)量控制,隨著中國(guó)加入ICH,和國(guó)際藥品監(jiān)管體系接軌,對(duì)藥品質(zhì)量和生產(chǎn)過程有了越來越嚴(yán)格的要求.
Ⅱ
蛋白A親和層析以及工藝優(yōu)化
目前單抗在純化階段多采用三步層析純化策略,ProteinA親和層析因?yàn)槠涓咛禺愋裕蔀榈谝徊酱旨兊氖走x。
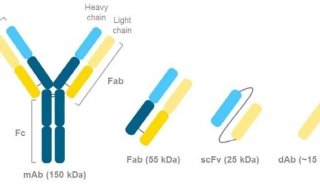
ProteinA是一種分離自金黃色葡萄球菌的細(xì)胞壁蛋白,通過Fc片段結(jié)合哺乳動(dòng)物IgG。天然的ProteinA不穩(wěn)定,將其改造后獲得的ProteinA不僅穩(wěn)定性更好,而且對(duì)Fc片段的結(jié)合能力更強(qiáng),非特異性結(jié)合更弱。將這種蛋白結(jié)合到微球上,便獲得了一種能夠特異性結(jié)合抗體蛋白的層新填料。SpreX ProA系列產(chǎn)品中結(jié)合的PeoteinA蛋白是經(jīng)過改造后的蛋白,可耐受高達(dá)0.5M NaOH,實(shí)現(xiàn)在使用結(jié)束后對(duì)填料更加徹底的清潔消毒。
以等電點(diǎn)在8左右的抗體蛋白為例,一般的粗純流程如下:
培養(yǎng)收獲液經(jīng)澄清過濾或離心分離后去除大的細(xì)胞和細(xì)胞碎片,再用0.45/0.22um的濾膜過濾,以使樣品能夠順利通過而不至于堵塞層析柱,隨后便可將進(jìn)行Pro A親和層析。層析中用到的所有緩沖液都要用0.45/0.22um的濾膜過濾,盡可能減少不溶性微粒,并降低微生物限度以減少使用過程中填料的損傷。典型的ProA親和層析步驟包括:

第一步
消毒是為了清洗雜質(zhì),排除上一次使用對(duì)本次層析的干擾,一般為0.1M NaOH,淋洗2CV后暫停15min。NaOH清洗填料的同時(shí)也會(huì)對(duì)填料造成不可逆的損傷,使用更加耐堿的SpreX ProA系列填料可使填料使用壽命更長(zhǎng)。
第二步
平衡是為了洗去NaOH,并將層析柱中的pH、電導(dǎo)等替換為與樣品接近的環(huán)境,使樣品結(jié)合更加穩(wěn)定。建議使用和澄清過濾時(shí)相同的平衡緩沖液,并平衡至pH、電導(dǎo)與平衡液相同。
第三步
上樣即為將樣品流過層析柱。在該過程中,應(yīng)選擇合適的樣品保留時(shí)間以使目的蛋白有充足的時(shí)間和填料中的ProteinA結(jié)合,通常建議保留時(shí)間4-6min,未結(jié)合的雜質(zhì)流穿。同時(shí),由于培養(yǎng)樣品一般粘度較高,上樣過程可能會(huì)有較大反壓,應(yīng)時(shí)刻注意壓力,保證在不超過最大壓力限制下上樣,此限制的優(yōu)先級(jí)應(yīng)高于保留時(shí)間對(duì)流速的要求。如壓力過大流速過低,解決方法可考慮通過一些手段先降低樣品粘性,或考慮使用粒徑更大的填料。
第四步
再平衡是使用與上樣前平衡時(shí)相同緩沖液將上樣結(jié)束后層析柱中還未流穿的雜質(zhì)頂洗出來。由于此過程中層析柱里仍然是樣品,還會(huì)有較大反壓,建議在第一個(gè)CV時(shí)使用同上樣時(shí)相同的流速,隨著樣品雜質(zhì)流穿后續(xù)可選擇使用更高流速,并直到pH、cond、uv280曲線平穩(wěn),一般需要5cv左右。
第五步
洗雜主要洗去填料上非特異性結(jié)合的雜質(zhì),一般使用pH5.5的緩沖液,并加入添加劑如氯化鈉、尿素等,通過高鹽來洗去雜質(zhì),洗去的雜質(zhì)主要包括HCP、DNA等。HCP結(jié)合在填料上的相互作用中 HCP與單抗之間的相互作用占主要部分,在酸性pH下抗體一般為中性或帶正電荷,而HCP大都為中性或帶負(fù)電荷,從而兩者之間容易形成疏水結(jié)合或者離子結(jié)合,通過中間pH和添加劑的緩沖液淋洗可以洗去一部分HCP雜質(zhì)。此外,由于不同添加劑作用不同,可以根據(jù)實(shí)際情況選擇合適的添加劑,目前氯化鈉是最常用的,但尿素、精氨酸等由于其不同的除雜機(jī)制,也被越來越多的使用。
第六步
平衡為pH5.5的洗雜時(shí)未加入添加劑的緩沖液,目的是將柱子內(nèi)緩沖液替換為低鹽條件,以防止洗雜緩沖液中加入的添加劑進(jìn)入洗脫樣品中,對(duì)蛋白穩(wěn)定性造成不利影響,同時(shí)也能洗去部分因疏水作用結(jié)合的HCP。
第七步
洗脫一般使用pH3.5左右的與上一步平衡時(shí)相同緩沖體系的緩沖液,利用低pH將目的蛋白洗脫,并在收集口收集樣品。若有相關(guān)需求,可在此時(shí)進(jìn)行低pH病毒滅活,若無相關(guān)需求,可直接用1M Tris-HCl,pH9.0調(diào)pH至蛋白穩(wěn)定的范圍,一般為5.5。回調(diào)過程中會(huì)出現(xiàn)沉淀,一般是HCP和核酸,也會(huì)有少量單抗聚集。再經(jīng)過深層過濾除去沉淀后HCP和核酸通常可降低至100ppm以下。有研究指出,在低pH下抗體蛋白會(huì)將疏水中心暴露出來從而導(dǎo)致聚集,而更加緩慢的調(diào)節(jié)pH,給蛋白更多的結(jié)構(gòu)變化時(shí)間能夠有效降低單抗的聚集。此外,也可以在洗脫緩沖液中加入適量氯化鈉從而可以在更加溫和的pH下將蛋白質(zhì)洗脫,或者加入適量乙二醇以減弱分子間疏水作用減少聚體的形成。
第八步
清洗一般使用1M HAc或0.1M Critic acid,目的是使用更低的pH將填料上未洗脫的其他雜質(zhì)洗脫下來。清洗的溶液pH建議大于2,以減少填料的損傷。如果仍然無法清洗干凈,可嘗試使用鹽酸胍、異丙醇清洗。
第九步
平衡是為了在第九步的氫氧化鈉消毒前有一個(gè)緩沖,否則酸堿直接中和會(huì)對(duì)填料有較大損傷。
第十步
消毒目的是利用0.1M NaOH的高pH將填料上的脂蛋白、脂質(zhì)和核酸洗脫,同時(shí)對(duì)填料進(jìn)行殺菌消毒,滅活細(xì)菌、病毒和內(nèi)毒素。
第十一步
平衡是為了將NaOH清洗干凈,防止對(duì)填料造成損傷。若無后續(xù)實(shí)驗(yàn),則可將填料保存于20%乙醇中。
Ⅲ
親和層析工藝優(yōu)化
樣品經(jīng)過一步層析后一般單體純度可達(dá)95%以上,收率為90%左右,主要雜質(zhì)為聚體、電荷異質(zhì)體、HCP、DNA和ProteinA。其中聚體和電荷異質(zhì)體等在親和層析階段優(yōu)化空間不大,另一方面是這些雜質(zhì)在后續(xù)離子層析階段可以去除,因此一般不作為親和層析工藝優(yōu)化關(guān)鍵點(diǎn)。Protein A是由于填料配基脫落所導(dǎo)致,一般只需維持在較低水平即可,而且也可以在離子層析階段去除,但其含量可作為填料自身性能變化的參考。因此,親和層析階段的工藝參數(shù)優(yōu)化應(yīng)重點(diǎn)關(guān)注收率、HCP、DNA和ProteinA.
樣品收率與樣品上樣載量密切相關(guān)。高流速、高載量是目前親和層析填料發(fā)展的趨勢(shì),選擇更高載量的填料以及合適的實(shí)際上樣載量能夠獲得更高的收率,同時(shí)降低生產(chǎn)成本。毫厘科技的SpreX ProA D80能夠在4min保留時(shí)間下達(dá)到60 mg hIgG/mL以上的動(dòng)態(tài)載量,其平均粒徑為80un,能夠?qū)崿F(xiàn)0.2MPa下500cm/h的流速,讓生產(chǎn)過程更加高效。SpreX ProA H60則粒徑更小,載量更高,為工藝開發(fā)帶來更多選擇。填料的高動(dòng)態(tài)載量還應(yīng)結(jié)合實(shí)際的工藝參數(shù),過高或過低的上樣載量都會(huì)導(dǎo)致收率降低,因此從低載量填料更換為高載量填料,還應(yīng)進(jìn)行對(duì)應(yīng)的工藝優(yōu)化實(shí)驗(yàn)。隨著親和層析填料使用次數(shù)的增加,其微球表面附著的雜質(zhì)也會(huì)越來越多并降低目標(biāo)蛋白的載量。此外洗脫pH、收集峰位置也會(huì)影響收率,高的洗脫pH和窄的收集峰會(huì)降低收率,但可以提高產(chǎn)品質(zhì)量;低的pH和寬的收集峰會(huì)提高收率,但會(huì)使產(chǎn)品質(zhì)量降低。工藝條件的優(yōu)化目標(biāo)是在質(zhì)量和收率之間的平衡,即在保證質(zhì)量的情況下盡可能提高收率。
目前抗體蛋白主要采用真核細(xì)胞胞外表達(dá),HCP和DNA會(huì)在培養(yǎng)末期或離心過程中細(xì)胞死亡后釋放出來,通常在親和層析前其含量可能高達(dá)幾十萬(wàn)甚至上百萬(wàn)ppm,而在親和層析后則下降到幾百ppm。HCP和DNA在pH5.5左右時(shí)一般帶負(fù)電荷,可回調(diào)pH后通過深層過濾去除,若對(duì)質(zhì)量有更高要求也可通過陰離子層析去除,同時(shí)陰離子層析還能去除核酸和病毒,且由于單抗的陰離子層析通常是流穿模式層析,工藝相對(duì)簡(jiǎn)單,被普遍應(yīng)用于單抗的純化。
親和后樣品中含有的ProteinA一般來源于親和填料配基的脫落,其一方面作為產(chǎn)品雜質(zhì)應(yīng)當(dāng)被控制,另一方面也可作為填料配基脫落程度的參考。使用SpreX ProA系列填料進(jìn)行親和層析,Protein A的含量可保持在10ppm以下。一般對(duì)填料配基脫落影響最大的因素是CIP階段的氫氧化鈉清洗。為了洗去填料上未洗脫的脂蛋白,滅活內(nèi)毒素以及控制微生物限度,一般會(huì)在層析前和層析后使用0.1M NaOH進(jìn)行15min左右的消毒,這對(duì)親和層析填料來說是必須的,但會(huì)極大影響配基的穩(wěn)定性,SpreX ProA系列填料使用經(jīng)改良的Protein A配基,能夠耐受0.5M NaOH,增加在0.1 M NaOH下的使用壽命。
以當(dāng)前純化工藝發(fā)展情況,親和層析填料通常占據(jù)所有層析填料成本50%左右,在當(dāng)下制藥行業(yè)整體降本增效的背景下,國(guó)產(chǎn)化已成為趨勢(shì)。毫厘科技全球領(lǐng)先的微流控微液滴成球技術(shù)過程可控,并且能夠制造出粒徑更加均一的微球,使用SpreX ProA系列填料將可能在樣品收集階段的分辨率、收集體積帶來更好的表現(xiàn),從而降低后續(xù)純化階段生產(chǎn)成本。
Ⅳ
填料動(dòng)態(tài)載量測(cè)試
填料動(dòng)態(tài)載量測(cè)試一般是在上樣載量?jī)?yōu)化或填料壽命驗(yàn)證中進(jìn)行。使用純化后的目標(biāo)蛋白測(cè)試不經(jīng)過層析柱時(shí)的uv值,隨后上樣直至有樣品流穿并且uv值達(dá)到10%流穿時(shí)的uv值,記錄上樣體積并計(jì)算填料載量。在親和層析工藝優(yōu)化時(shí),通常樣品上樣載量定為動(dòng)態(tài)載量的80%左右。在親和層析填料壽命驗(yàn)證階段,當(dāng)動(dòng)態(tài)載量出現(xiàn)明顯下降時(shí)的使用次數(shù)定為壽命終點(diǎn)。
Ⅴ
親和層析中的ProteinA的替代品
為了滿足高性價(jià)比產(chǎn)品的巨大需求,同時(shí)滿足嚴(yán)格的質(zhì)量標(biāo)準(zhǔn),對(duì)生產(chǎn)策略進(jìn)行了必要改進(jìn),人們?cè)O(shè)計(jì)并研究了蛋白A的替代配體。蛋白質(zhì)G和蛋白質(zhì)L是已知的與蛋白質(zhì)A功能相似的配體。蛋白質(zhì)G由一個(gè)多肽組成,多個(gè)結(jié)合域以圓柱形連接;蛋白G由1個(gè)具有多個(gè)結(jié)合域的單肽組成,來源于G群和C群鏈球菌。然而,ProteinG比ProteinA沒有太大的優(yōu)勢(shì),最重要的限制是洗脫的pH太低,非特異性行為升高,聚集體含量高,穩(wěn)定性下降,綜合成本甚至高于ProteinA 樹脂。ProteinL也是由鏈球菌表達(dá),會(huì)與包含特定kappa輕鏈的抗體特異性結(jié)合,由于其高特異性,蛋白L在單抗純化過程中尚未取代ProteinA。
ProteinA并不能結(jié)合所有IgG,而且有的抗體蛋白中并不含有Fc段,因此會(huì)有基于ProteinL或其他親和配體的親和層析。但這些產(chǎn)品仍需在載量、穩(wěn)定性等方面改進(jìn)才能使性能超過基于ProteinA的親和層析。

? ? ?關(guān)于毫厘科技
毫厘科技致力于微流控生產(chǎn)型芯片開發(fā),為生命科學(xué)微球材料提供高通量數(shù)字化生產(chǎn)平臺(tái),用于多種類型的納微級(jí)別功能性微球和生物粒子的分選、制造與工業(yè)級(jí)連續(xù)生產(chǎn),可兼容瓊脂糖、無機(jī)材料、聚合物等不同材質(zhì)及不同尺寸不同結(jié)構(gòu)的特殊要求。
產(chǎn)品廣泛應(yīng)用于生物制藥純化工藝、藥物包裹與遞送、單細(xì)胞篩選、體外診斷和醫(yī)美材料等領(lǐng)域,持續(xù)為生命科學(xué)客戶提供穩(wěn)定的高品質(zhì)產(chǎn)品和定制化微球解決方案,加速研發(fā)進(jìn)度,提高生產(chǎn)效率、優(yōu)化成本結(jié)構(gòu)。
往期推薦