抗體偶聯藥物(ADC)分析的新利器
藥物/抗體比率(DAR)是抗體偶聯藥物(ADC)的一種關鍵質量屬性(CQA),因為它直接影響ADC的治療效果和藥代動力學。在ADC開發過程和商業化生產運營中,DAR的測定和監測至關重要。

非變性電噴霧質譜(非變性質譜)已成為分析共價復合蛋白質治療藥物和非共價蛋白質復合體的有力工具。但非變性質譜面臨多種獨有的難題,包括在嘗試使用注入式MS時,需要在分析前進行大量樣品凈化,并要求操作人員擁有更高的技術水平以獲得并解析實驗結果。
接下來,小編將給大家介紹如何采用BioAccord系統來改善非變性質譜法分析半胱氨酸偶聯ADC和賴氨酸偶聯ADC的易用性。
沃特世解決方案
 《聽分析科學家們談論全新BioAccord系統》
《聽分析科學家們談論全新BioAccord系統》
半胱氨酸偶聯ADC分析采用非變性質譜分析法,需要在非變性條件下保持非共價連接的ADC分子完整,從而確定ADC樣品的DAR值和載藥量分布。本研究將BioAccord系統直接與分析型SEC色譜柱(ACQUITY UPLC BEH SEC蛋白分析專用柱, 200?, 1.7 μm, 2.1 mm × 150 mm,部件號186008471)聯用進行等度洗脫(50 mM醋酸銨(NH4OAc),運行時間10分鐘)。

圖1. 利用BioAccord系統進行非變性LC(SEC)-MS分析,在不經去糖基化處理的情況下得到標準品(mAb)以及低、中和高偶聯水平半胱氨酸偶聯ADC樣品的多電荷峰簇的組合原始譜圖(左圖)、組合原始譜圖的放大區域(單電荷態)(中圖)和解卷積譜圖(右圖)。比較三種不同半胱氨酸偶聯ADC樣品隨載藥量增加的藥物分布。

在無需進行樣品去糖基化的情況下,對賴氨酸偶聯ADC Kadcyla(曲妥珠單抗-美坦新偶聯物(T-DM1))進行LC(SEC)-MS分析獲得原始譜圖和解卷積譜圖(圖2)。
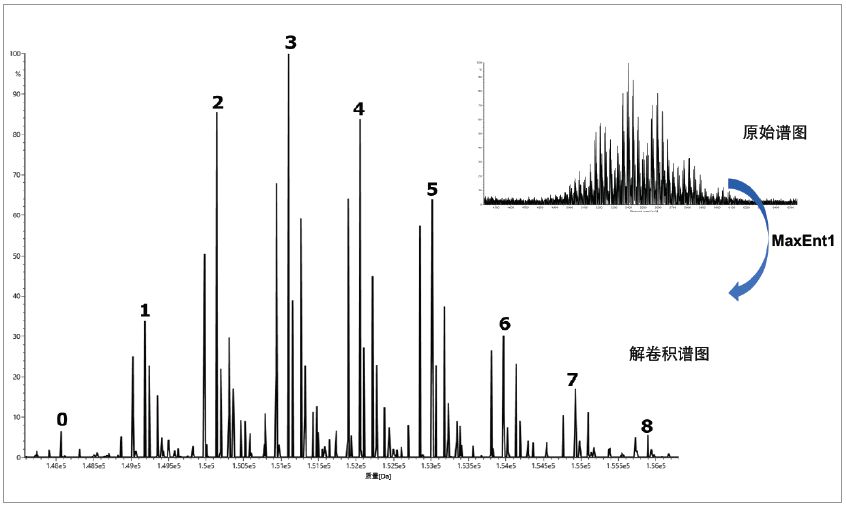
已有文獻詳細介紹過使用非變性質譜方法分析共價賴氨酸偶聯ADC的優勢。在解卷積譜峰上標記出檢測到的偶聯藥物數量。利用UNIFI計算得出的DAR值為3.46,與藥品生產商報告的DAR (3.50)較為一致。同樣,結果與之前使用Vion IMS QTof系統得到的研究結果相當。
總結來說,BioAccord系統非常適用于對半胱氨酸偶聯ADC和賴氨酸偶聯ADC進行LC(SEC)-非變性質譜分析。平均DAR和載藥量分布結果與疏水作用色譜(HIC)分離(配備TUV檢測)產生的結果以及利用前幾代QTof MS系統所得到的結果相當。
點擊文末“閱讀原文”,立即下載完整的應用紀要。

















